7 Termofysik: 7.1 Tryck
 Gastryck
Gastryck
Gastryck
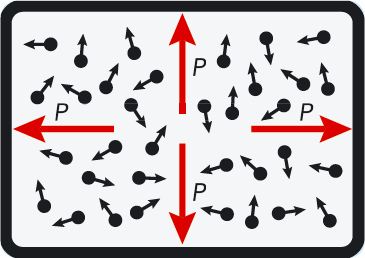
En gas är en enorm mängd molekyler i oupphörlig rörelse med hög hastighet i alla riktningar. Molekylerna kolliderar ständigt med varandra och med ytor som är i kontakt med gasen. Det gör att gasen i en behållare fyller hela behållaren och trycker på alla ytorna. Gasmolekylerna kolliderar ständigt med väggarna. Det ger gastrycket mot väggarna. Se figur 7.10.
Luftmolekylerna nederst i atmosfären ger ett lufttryck som vid havsytan har medelvärdet \(101 \ 325 \text{ Pa}\). Detta tryck kallar vi \(1\) atmosfär, \(1 \text{ atm}\). \[ 1 \text{ atm} = 101{,}3 \text{ kPa}\]
Lufttrycket mäter vi med en barometer.
En av de första som tillverkade en barometer och mätte atmosfärstrycket var italienaren Evangelista Torricelli (1608–1647). Han var Galileis efterträdare som professor i Pisa. Torricelli fyllde ett långt glasrör med kvicksilver, satte ett finger mot röröppningen och vände röret upp och ner. Sedan satte han ner röret i ett kar med kvicksilver. Se figur 7.11. Då han tog bort fingret, rann lite av kvicksilvret ut i karet, så att det uppstod vakuum längst upp i röret. Men kvicksilvret i röret stod \(760 \text{ mm}\) över kvicksilvret i karet. Hur förklarar vi det?
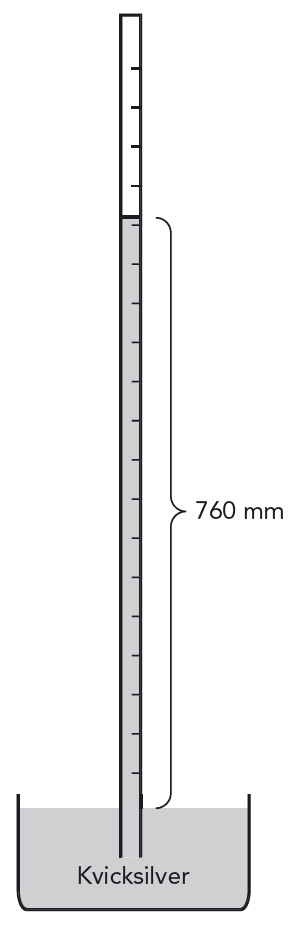
Trycket på den fria vätskeytan utanför röret måste vara lika stort som trycket på samma nivå inne i röret. Alltså måste lufttrycket vara lika stort som trycket av \(760 \text{ mm}\) kvicksilver. Vi kan också uttrycka det på följande sätt: Tyngden av hela atmosfären är lika stor som tyngden av ett \(760 \text{ mm}\) djupt kvicksilverhav utspritt över hela jorden.
I en vätska ökar trycket med djupet. Detsamma gäller för en gas. I atmosfären minskar därför lufttrycket med höjden. Det kan du märka i en hiss eller i ett flygplan som stiger snabbt. Det slår "lock för dina öron". Det beror på att lufttrycket på utsidan av trumhinnorna blir lägre än på insidan, så att trumhinnorna buktar utåt.
Pascals lag för vätsketryck, \(p = \rho gh\), kan inte användas på lufttrycket i atmosfären. Orsaken är att luftens densitet avtar med höjden.
Hur högt skulle atmosfären ha nått om luften hela vägen hade haft samma densitet som vid havsytan, \(1{,}29 \text{ kg/m\(^3\)} \)?
Lösning: Lufttrycket är \(p = 101{,}3 \text{ kPa}\) nederst och \(p_0 = 0\) överst. Formeln \(p = p_0 + \rho gh\) ger då \[ h = \frac{p}{\rho g} = \frac{101{,}3 \cdot 10^3}{ 1{,}29 \cdot 9{,}82} \text{ m} = 8{,}0 \text{ km} \]
Svaret är helt orealistiskt. Mount Everest och en del andra fjälltoppar skulle ha stuckit ut ovanför atmosfären! I verkligheten sträcker sig atmosfären mer än \(100 \text{ km}\) uppåt, men trycket och densiteten närmar sig noll.
Teoretiskt sett skulle du kunna använda ett drygt \(10 \text{ m}\) långt sugrör och suga upp läsk från din läskedrycksflaska \(10 \text{ m}\) ovanför den. Hur långt sugrör skulle du kunna använda på månen?
Lösning: Först måste vi klara ut vad som händer när vi dricker ur ett sugrör. Innan du har börjat suga verkar lufttrycket likadant överallt och därför är vätskenivån lika i läskflaskan och i sugröret. När du suger ut luften ur sugröret blir det ett lägre tryck i sugröret. Eftersom trycket nu är större utanför sugröret än inuti trycker luften på vätskeytan och pressar på så sätt upp läsken i sugröret. Så är det på jorden, men på månen finns det ingen atmosfär och därmed inte heller något lufttryck. Därför går det inte alls att dricka läsk genom ett sugrör på månen!
Försök att visa varför du bara kan använda ett sugrör som är drygt \(10 \text{ m}\).


